Termoquímica
Os tipos de energia utilizada nas ligações é o Joule (J), quilojoule (KJ), caloria (cal) ou quilocaloria (Kcal).
Devemos lembrar que 1 caloria corresponde a 4,18 joules.
O valor da energia nas ligações, absorvida (endotérmica) ou liberada (exotérmica) é medida por cada mol da substância.
Devemos lembrar que um mol de qualquer substância, envolve o número de partículas de 6,02 x 1023 partículas da substância.
Deve-se também levar em conta a pressão e a temperatura padrão de cada reação. A pressão deve ser de 1 atmosfera e a temperatura de 25ºC.
Energia Térmica Nas Ligações Químicas
Energia de Ligação
É a energia absorvida pelas substâncias no estado gasoso, quando um mol das ligações entre seus átomos componentes se rompem.
Exemplos de Ligações Entre os Átomos de Uma Molécula.
Gás Hidrogênio
Uma ligação covalente molecular une os dois átomos de hidrogênio, para formar o gás hidrogênio.
Uma ligação covalente molecular une os dois átomos de hidrogênio, para formar o gás hidrogênio.
Gás hidrogênio A ligação covalente molecular
Água
Duas ligações covalentes moleculares simples, unem dois átomos de hidrogênio ao oxigênio para formar a água.
Água Ligações covalentes moleculares
Água oxigenada
Três ligações covalentes moleculares simples unem dois átomos de hidrogênios com dois átomos de oxigênio para formar a água oxigenada.
Água oxigenada ligações covalentes moleculares
Gá metano
Quatro ligações covalentes moleculares simples, unem 4 hidrogênios ao carbono central para formar o gás metano.
Gás metano ligações covalentes moleculares
Gás Etano
Seis ligações covalentes moleculares simples, unem 6 hidrogênio a dois carbonos ligados entre si por uma única ligação simples para formar o gás etano.
Gás etano ligações covalentes moleculares
Gás butano
Dez ligações carbono - hidrogênio e três ligações carbono - carbono formam a estrutura do gás butano, (gás engarrafado de cozinha).
Gás butano 10 ligações C---H e 3 ligações C---C
Álcool etílico
Cinco ligações carbono - hidrogênio, uma carbono - oxigênio, uma oxigênio - hidrogênio, formam a estrutura molecular do álcool etílico.
5 ligações C---H, 1 ligação C---O, 1 ligação O---H
Energia Das Ligações
Energia de formação das moléculas
Os dois hidrogênios que formam esse gás, possui energia de ligação de 437 kJ/mol.
Gás Etano
Seis ligações covalentes moleculares simples, unem 6 hidrogênio a dois carbonos ligados entre si por uma única ligação simples para formar o gás etano.
Gás butano
Dez ligações carbono - hidrogênio e três ligações carbono - carbono formam a estrutura do gás butano, (gás engarrafado de cozinha).
Gás butano 10 ligações C---H e 3 ligações C---C
Álcool etílico
Cinco ligações carbono - hidrogênio, uma carbono - oxigênio, uma oxigênio - hidrogênio, formam a estrutura molecular do álcool etílico.
5 ligações C---H, 1 ligação C---O, 1 ligação O---H
Energia Das Ligações
Energia de formação das moléculas
Os dois hidrogênios que formam esse gás, possui energia de ligação de 437 kJ/mol.
Duas ligações hidrogênio - oxigênio de 461 kJ cada, formam a molécula de água.
Energia das Combustões
Nas transformações químicas são quebrados e formados novos materiais, nesse rearranjo da matéria; ligações entre átomos são rompidas e outras são formadas, com absorção ou liberação de energia térmica. Cada ligação química tem um valor térmico conhecido específico. Esses valores podem ser representados numa tabela.
Tabela dos Valores das Ligações Químicas
Exercícios
15) O gás metano tem origem nos vulcões, na decomposição de lixo orgânico, ou dos vegetais, folhas, troncos em apodrecimento, é produzido no intestino de animais herbívoros, e até nós humanos produzimos no nosso intestino, por meio de bactérias do tipo Escherichia coli, há traços desse gás presente na atmosfera terrestre, que com o seu aumento causa o efeito estufa, está contido no gás natural, ou no biogás, ou pode se obter juntamente com o petróleo. Atualmente está sendo utilizado como gás canalizado de cozinha e combustíveis para veículos automotores.
17) Qual o total da energia envolvida nas ligações rompidas, dos reagentes metano e do gás oxigênio?
18) Qual o total da energia envolvida, liberada; nas ligações formadas dos produtos da combustão do gás metano (CH4)?
19) Qual a energia liberada, ou o saldo de energia fornecida na combustão de um mol de gás metano?
A chama que sai da boca do fogão e aquece a panela, é o saldo da energia 814 kj/ mol, da combustão do gás metano (CH4).
20) O gás propano, C3H8, é um dos componentes do GLP, gás liquefeito de petróleo. Escolha abaixo a equação correta que representa a combustão desse gás e assinale.
a) 1 C3H8 + 3 O2 ---combustãoà 3 CO2 + 2 H2O
b) 2 C3H8 + 5 O2 ---combustãoà 2 CO2 + 5 H2O
c) 1 C3H8 + 5 O2 ---combustãoà 3 CO2 + 4 H2O
d) 1 C3H8 + 4 O2 ---combustãoà 2 CO2 + 4 H2O
e) 2 C3H8 + 3 O2 ---combustãoà 3 CO2 + 4 H2O
Energia De Ligação Das Moléculas
Ligações do gás hidrogênio (H2)
A molécula do gás hidrogênio possui 1 ligação H --- H, cuja energia de ligação é 436 KJ/mol.
Como sabemos que a energia medida para cada 1 mol de gás hidrogênio, então: qual é a energia de ligação envolvida nas ligações de 20 gramas de gás hidrogênio (H)2?
Ligações da molécula de água
A molécula de água é formada por 2 ligações O --- H, cuja energia de ligação é 463 KJ/mol, com um total de energia de 926 KJ/mol.
Ligações da água Oxigenada
A água oxigenada é formada por 2 ligações H ---O, cuja energia de ligação é 463 KJ/mol e 1 ligação O --- O, cuja energia é 134 KJ/mol, cuja energia total envolvida é de 1064 KJ/mol.
Ligações do Gás Metano
O gás metano é formado por 4 ligações C --- H cuja energia de ligação é 413 KJ/mol, com um total de energia envolvida de 1652 KJ/mol.
Ligações do gás Etano
O gás etano é formado por 6 ligações H --- C, cuja energia de ligação é 412,9 KJ/mol e 1 ligação C --- C cuja energia de ligação é 347,8 KJ/mol, com um total de 2437,6 KJ/ mol envolvido.
Ligações do Gás Butano
Energia de ligação do gás butano (C4H10)
A molécula do gás butano é formada por 3 ligações C --- C, cuja energia de ligação é 348 KJ por mol e 10 ligações C --- H, cuja energia de ligação é 412 KJ/mol formado, com um total de 5164 Kj/mol formado.
Exemplo
Ligações do etanol
A molécula do etanol é formada por 1 ligação C --- C, cuja energia de ligação é 348 KJ/mol, 6 ligações H --- C cuja energia de ligação é 413 KJ/mol, 1 ligação C ---O, cuja energia de ligação é 357 KJ/mol e 3 ligações O --- H cuja energia de ligação é 462 KJ/mol, com um total de 4569 KJ/mol formado.
Exemplo
Energia de Rompimento das Ligações
Absorção de Energia
A energia do rompimento ou quebra das ligações de uma molécula é a mesma energia das ligações das moléculas e é sempre positiva; portanto é endotérmica. geralmente o valor da energia é acompanhado pelo sinal de mais (+).
A energia utilizada na "quebra das ligações" é a energia gasta para cada mol de ligação.
Essa energia é medida sempre para 1 mol da substância que sofre rompimento de suas ligações.
Rompimento da ligação do gás hidrogênio.
Como o rompimento é de um mol do gás Hidrogênio ou de 2 gramas desse gás e corresponde a 436 Kj/mol ou 104,3 Kcal/mol e irá liberar dois mols de H atômico gasoso.
No caso de se querer saber sobre a quebra de apenas 1
grama ou ⅟2 mol de gás
hidrogênio, quanto de energia iria necessitar para romper as ligações?
No caso de se querer saber sobre a quebra de apenas 5 gramas ou 2,5 mol de gás
hidrogênio, quanto de energia iria necessitar para romper as ligações?






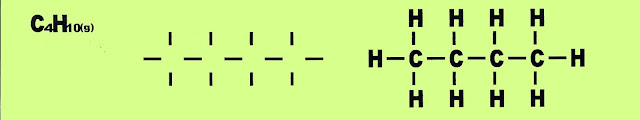




















Nenhum comentário:
Postar um comentário